
En géologie ou en paléontologie, on arrive à déterminer l’âge des fossiles à partir de la « méthode au carbone 14 ».
Cela peut sembler mystérieux et compliqué, mais en réalité c’est une méthode très simple. Sur le principe, c’est une sorte de sablier moléculaire : certains atomes quittent le fossile avec le temps, et il s’agit ici de compter ceux qui restent pour en déduire l’âge.
Le carbone… 14 ?
Dans le cas de la datation au carbone 14, l’atome dont on mesure la quantité présente est le carbone 14 (noté 14C), un atome de carbone qui possède un excès de deux neutrons par rapport à son homologue (son isotope) habituel, le carbone 12 (noté 12C).
Le 14C reste du carbone et il est utilisé de façon transparente par les êtres vivants et il se retrouve ainsi intégré dans les tissus organiques.
La particularité du 14C c’est qu’il se désintègre spontanément : il est radioactif. Ceci est dû à la structure instable du noyau de cet atome, qui ne lui permet pas de rester tel quel (à cause notamment de l’interaction faible qui agit à ces échelles).
Cette désintégration se traduit par une transformation de l’atome de 14C en azote 14 (un des neutrons excédentaire du 14C devient un proton et libère un électron). La désintégration des atomes radioactifs comme le 14C se fait selon une vitesse bien précise.
La décroissance du carbone 14
Si l’on enferme du carbone dans un bocal, alors la quantité de 14C dans le bocal décroît naturellement.
Ceci est également ce qui se produit ici : du 14C, accumulé par l’organisme durant sa vie, est emprisonné dans le fossile et sa quantité diminue avec le temps. C’est alors en mesurant ce qu’il reste que l’on arrive à déterminer l’âge du fossile.
Dans l’air (celui que les êtres vivants respirent), il existe environ 1 atome de 14C pour mille milliards d’atomes de 12C. C’est relativement peu, mais largement assez pour travailler avec.
La vitesse de désintégration suit la loi très simple suivante : tous les 5 730 ans, il a 50 % du 14C restant qui a disparu. La durée de 5 730 ans est appelée la demie-vie du 14C.
Ainsi :
- 5 730 ans après la mort d’un être vivant, il reste 50 % de son capital de 14C ;
- après 11 460 ans, il reste 25 % ;
- après 17 190 ans, il reste 12,5 % de 14C :
- etc.
On traduit ceci par une courbe de décroissance :
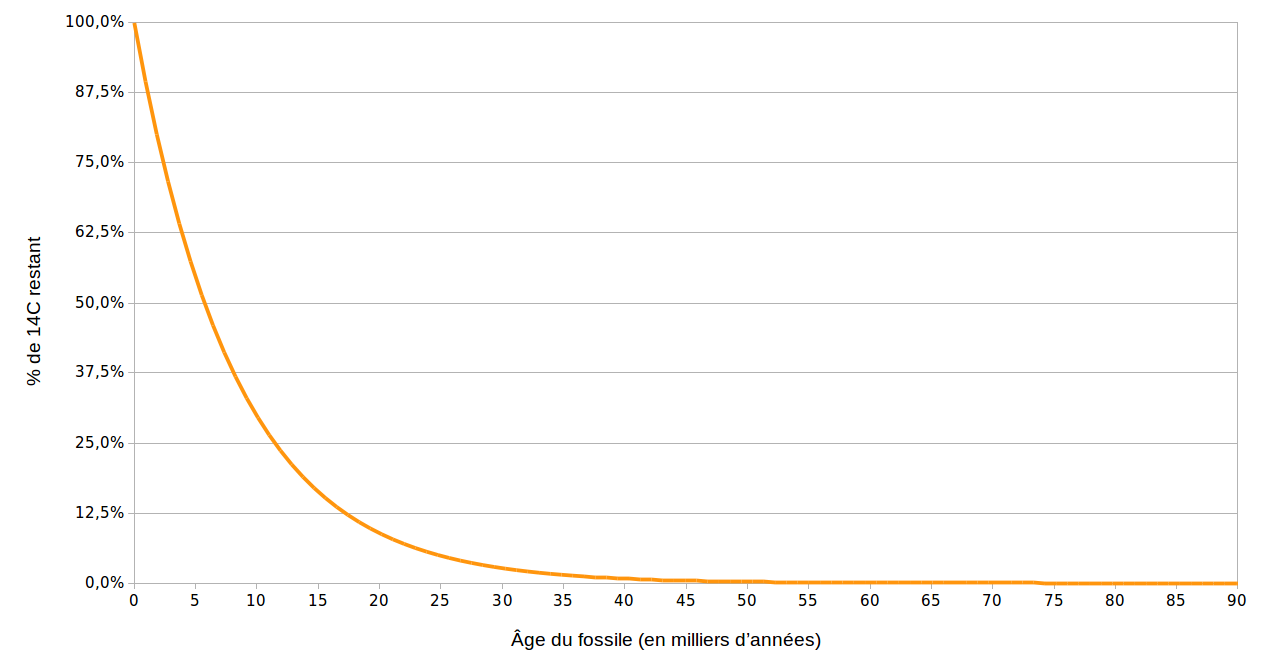
Connaissant le taux de 14C dans un fossile, on détermine alors son âge. Facile, non ?
Les limites de cette méthode de datation
Si vous prenez un sablier et que vous l’oubliez, tout le sable sera tombé : si vous n’avez pas noté l’heure où vous l’aviez retourné, il est impossible de savoir à quelle heure le sable s’est arrêté de tomber. Pour le 14C, c’est pareil : quand il n’y a plus de 14C du tout, ou trop peu pour avoir une mesure fiable, alors on ne peut plus connaître l’âge du fossile.
La datation au carbone 14 est fiable pour les fossiles organiques qui ont jusqu’à 50 000 ans. Au-delà il faut utiliser une autre méthode de datation : datation à l’uranium selon le même principe, par exemple, qui a une demie-vie beaucoup plus longue de 700 millions d’années.
Une autre limite du 14C, c’est qu’il se base sur le fait que, au moment de la mort d’un organisme, le taux de 14C qu’il contient correspond à celui dans l’atmosphère. Ce taux atmosphérique a été relativement constant au fil des ères, jusqu’à environ 1950. En effet, c’est à cette période que l’humanité a commence à pratiquer un grand nombre d’essais nucléaires. Ceci a libéré des quantités importantes de 14C artificiel et toute mesure par cette méthode de l’âge d’un organisme mort après 1950 serait faussée.
De plus, la datation au 14C, vous le comprendrez, ne peut fonctionner que pour les fossiles d’être vivants. Pour dater un minéral, ce n’est pas possible (le rocher ne respire pas et ne renouvelle son quota de 14C durant son existence). Pour dater une roche, les scientifiques utilisent plutôt la datation à l’uranium, la datation par thermoluminescence ou une méthode utilisant la rémanence du champ magnétique terrestre.
Enfin, on peut remarquer que depuis la formation de la Terre, tout le 14C initialement formé devrait avoir disparu, et c’est vrai.
Mais c’est sans compter qu’il se forme constamment du 14C dans l’atmosphère, grâce aux rayons cosmiques. L’atmosphère est majoritairement composée d’azote, et quand un rayon cosmique heurte un atome d’azote, l’énergie de la collision peut transformer un des protons de l’azote en un neutron (et une autre particule appelée positron). L’atome devient du carbone, et plus précisément du 14C. Le flux de rayonnement cosmique permet donc de renouveler le carbone qui se désintègre.