
Ils sont instables, explosifs, corrosifs ou oxydants : certains produits chimiques sont tellement puissants qu’ils nécessitent d’importantes précautions d’emploi, même pour les professionnels.
L’hydrogène
Composant des 3/4 de l’univers connu, l’hydrogène est sur Terre un gaz explosif, détonant et très combustible. Il s’associe avec l’oxygène de l’air pour former de l’eau et libérer une importante quantité d’énergie (mise à profit dans les boosters des fusées).
Dans la bombe à hydrogène (bombe H), la plus puissante bombe créée par l’homme, ce n’est pas sa réactivité chimique qui est utilisée, mais un mécanisme de fusion thermonucléaire.
La nitroglycérine

Classique : ce composé liquide de formule C3H5(NO3)3 explose en formant plusieurs gaz, dont le dioxyde de carbone, le diazote, du dioxygène et l’eau. Si son explosion est si importante c’est en partie à cause de la grande quantité de gaz produits : plus de 1000 fois le volume de gaz par rapport au volume liquide.
La nitro est également très instable mécaniquement : un choc peut détruire la fragile molécule et libérer de la chaleur pour produire une réaction en chaîne. En revanche, des bâtons de sable ou du carton imbibé de nitro sont stables : sous cette forme, c’est de la dynamite. Il peut alors être transporté et même jeté au feu sans que ça n’explose. Pour le faire péter, il faut une onde de choc, telle qu’une étincelle. Ce procédé, breveté par Alfred Nobel, à la fin du 19ᵉ siècle, lui permis d’acquérir une immense fortune, dont les seuls intérêts suffisent encore aujourd’hui à distribuer les fameux prix Nobel.
L’oxygène liquide
L’oxygène est un comburant : il permet une combustion. Sa forme gazeuse pure est déjà suffisamment concentrée pour réactiver instantanément la flamme d’une allumette simplement incandescente. L’oxygène liquide est chimiquement 1 485 fois plus concentré et a donc un pouvoir oxydant plus important. Certains produits explosent à son contact, comme ce coton imbibé d’où l’on approche une flamme.
L’ozone, ou tri-oxygène, est encore plus corrosif que le dioxygène normal.
Le tri-iodure d’azote

Ce produit, sous sa forme solide, est des plus instables : un simple effleurement par une plume suffit à produire sa détonation. Sous sa forme dissoute dans l’eau il ne pose pas de problèmes, mais l’endroit où il sèche sera forcément l’endroit où il va exploser. Il est impossible de le transporter, car le moindre choc provoque son explosion : même une particule cosmique ou un bruit un peu fort peuvent déclencher l’explosion.
Le difluore
La plupart des produits chimiques sont conservés dans du verre, car ce dernier est assez peu oxydable. Le difluor est un des gaz si corrosifs qu’il attaque le verre. Le fluor est ce qu’on appelle « électronégatif » ce qui signifie qu’il est en manque d’électron. Attaquer un matériau pour lui prendre un électron est sa façon de se stabiliser.
Le fluor attaque l’intégralité du tableau périodique à la seule exception des deux éléments les plus stables : l’hélium et le néon. Même le platine ou l’or ne sont épargnés.
Une des façons de le stocker est d’utiliser un récipient en nickel oxydé : la couche d’oxydation arrive à stopper la corrosion par le fluor.
N’importe quel matériau s’enflamme instantanément au contact de ce gaz : papier, coton, bois, acier.
On trouve du fluor dans le dentifrice ou le sel de table, mais il n’est pas pur. Car une fois que le fluor a trouvé un électron, il est stable et ne présente aucun danger. Dans le dentifrice, il oxyde les dents pour se fixer dessus, empêchant les bactéries de le faire et protégeant ainsi la dent.
Le difluorure de dioxygène

Le difluore ci-dessus est déjà exceptionnellement réactif, et le dioxygène — celui que l’on respire — l’est mine de rien également. Quand on met les deux ensemble et que l’on chauffe, ils se réarragent une seule molécule de O2F2, ou F-O-O-F, parfois appalée simplement FOOF.
Ce matériau est un des plus puissants oxydants connus et il arrive à décomposer à peu près n’importe quoi, même à des températures cryogéniques et à l’état solide. Il fait exploser de la glace d’eau, du méthane liquide et même l’ammoniac.
Il est très instable et se décompose même à des températures de −160 °C en dioxygène et difluores, eux-mêmes encore très réactifs. Il n’a à ce jour pas d’applications connues, car il est impossible de le conserver de façon sécurisée : nombre d’expériences parmi lesquelles le FOOF est intervenu ont fini en incendies et explosions…
(merci à Théo pour m’avoir partagé cette molécule là !)
L’eau régale
L’eau régale est le seul acide (sauf les superacides) capable de dissoudre l’or. C’est un mélange d’acide chlorhydrique d’acide nitrique concentré. L’acide nitrique arrive à retirer un atome d’or, et l’acide chlorhydrique arrive à le prendre à l’acide nitrique, pour qu’il en retire un autre, et ainsi de suite.
Les deux acides pris de manière séparée n’arrivent pas à dissoudre l’or, ce qui est d’autant plus intéressant d’un point de vue chimique.
L’acide fluoroantimonique

C’est le superacide le plus fort connu à ce jour. Il est dix mille millions de milliard de fois plus puissant que l’acide sulfurique à 100 % ! L’étudier est assez difficile en raison de ça, vu qu’il dissout tout ce qui entre en contact avec lui. Il est par ailleurs très difficilement conservable, et seul le téflon peut s’en charger.
La thermite et la thermate
La thermite est un mélange d’aluminium et d’oxyde de fer tous les deux en poudre. Sa particularité est de générer une chaleur plus qu’intense atteignant les 2 500 °C. Cette vidéo le montre à l’œuvre en train de fondre à travers un bloc moteur, en quelques secondes. La thermate contient en plus du soufre par rapport à la thermite, qui augmente encore plus ses effets.
Le potassium métallique
Le potassium, comme le sodium ou le césium et tous les éléments solides de la première colonne du tableau périodique réagissent violemment au contact de l’eau : ils s’enflamment et explosent, libérant de l’hydrogène qui va lui aussi exploser. Le produit qui reste est, dans ce cas, une solution d’hydroxyde de potassium : un agent très corrosif.
L’octonitrocubane

C’est une belle molécule en forme de cube avec à chaque coin un groupe nitro NO2. Il s’agit de l’explosif non-nucléaire le plus puissant au monde, mais qui malgré cela est extrêmement résistante et stable : il peut être chauffé à 200 °C et percuté avec un marteau sans qu’elle explose. Sa synthèse est cependant difficile, et la production à grande échelle n’est pas encore possible.
Le trifluorure de chlore
Ce produit est corrosif, toxique (il dissout la chair et les os), explose au contact de l’eau, entre en ébullition exposée à l’air et brûle à plus de 2 400 °C. Il a été mis au point par les Nazis avant la seconde guerre mondiale, mais fut rapidement abandonné car trop dangereux et délicat à manipuler.
Il est tellement instable qu’il dissout le béton et réagit vivement si le récipient qui le contient n’est pas propre.
Le diazide de (5-azido-1H-tétrazol-1-yl)-carbamimidoyle
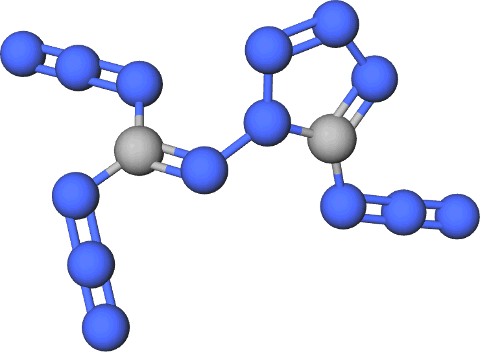
Souvent, une molécule carbonée qui contient beaucoup d’atome d’azote est aussi un puissant explosif. C’est le cas de la nitroglycérine, ou de l’octonitrocubane vu ci-dessus. La présente molécule (azidoazide azide en anglais, et dont j’ai dû recréer le nom français avec un peu d’aide) contient quatorze atomes d’azote pour deux atomes de carbone, ce qui en fait l’un des explosifs les plus puissants au monde, mais contrairement à l’octonitrocubane et à l’instar du tri-iodure d’azote, il est très instable ! Il explose aux chocs, au bruit, quand on allume la lumière, le place en solution et même… sans aucune raison particulière.
Le tétraazidométhane
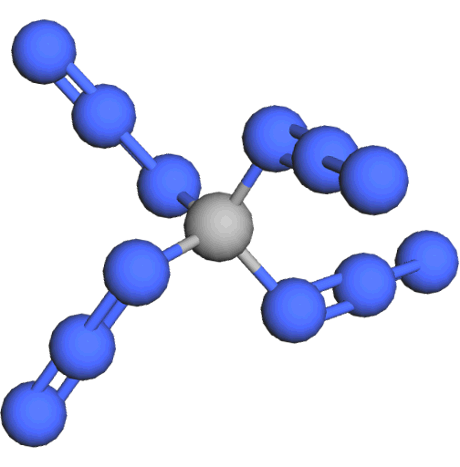
Prenez un atome de carbone et collez-lui 4 groupes d’azoture instable N3 : vous avez formé du tétraazidométhane, la molécule organique avec la plus haute concentration en azote, et l’une des plus denses en énergie !
Il est dit qu’une seule goutte de ce produit peut faire péter le récipient qui le contient, en plus de la hotte de protection sous laquelle on le manipule.
Lien :
(Cet article a initialement été publié sur Le Hollandais Volant. J’ai décidé de le déplacer ici, avec ses commentaires)