
On parle des « trois états de la matière » que sont le solide, le liquide et le gaz. Il en existe pourtant d’autres : peut-être connaissez-vous le plasma ? Mais avez-vous déjà entendu parler de l’état supercritique (à ne pas confondre avec le superfluide, qui en est encore un autre) ?
L’état supercritique n’est pas rencontré dans la vie courante, mais il est fort possible que vous ayez des choses chez vous dont la fabrication ait impliqué des fluides supercritiques.
État supercritique
Si l’on observe le diagramme des phases d’un corps on note deux points remarquables : le point triple, qui est le point pression-température où ce corps peut exister à la fois sous sa forme solide, liquide et gazeuse, et le point critique :
C’est le point critique qui nous intéresse, car si on le dépasse, le corps devient un fluide supercritique (super = « au-dessus », [du point] critique). Un fluide supercritique ne peut donc exister qu’à des hautes pressions et des hautes températures.
Pour expliquer ce qu’est un fluide supercritique et comment le produire, faisons une expérience de pensée.
Imaginez une bouteille que vous remplissez à moitié d’eau. À ce stade, la bouteille est remplie à moitié d’eau et moitié d’air. Pour notre expérience, il faut commencer par chasser l’air : pour cela, on branche la bouteille à une pompe à vide qui va chasser cet air.
On va supposer que la bouteille ne se déforme pas : on se retrouve alors avec une bouteille contenant 50 % d’eau et 50 % de vide au-dessus. Sauf que, la pression ayant baissé, l’eau va se mettre à bouillir et de l’eau gazeuse (eau sous sa forme de gaz, pas de l’eau gazéifiée et avec des bulles) va combler le vide. À ce moment, la bouteille ne contient que de l’eau dans les états liquides et gazeux.
Rappelons que dans un gaz, les molécules sont libres et espacées les unes des autres. Dans un liquide, les molécules sont toujours libres, mais rapprochées les unes des autres :

Maintenant, on va chauffer la bouteille.
Sous l’effet de la température, une partie du liquide va s’évaporer et devenir du gaz. Comme il y a maintenant davantage de gaz, les molécules sont moins espacées : la pression augmente. La densité du gaz, au passage, augmente aussi.
Parallèlement, la température va dilater le liquide : les molécules dans le liquide vont s’agiter davantage et ces dernières vont prendre globalement plus de place :

Si l’on chauffe suffisamment, la densité augmentant du gaz va rejoindre la densité diminuant du liquide : le gaz et le liquide obtiennent alors la même densité ! C’est à ce moment que la magie opère : les deux phases se mélangent et on obtient un fluide unique sans interface entre le gaz et le liquide ! On appelle ce fluide le fluide supercritique :
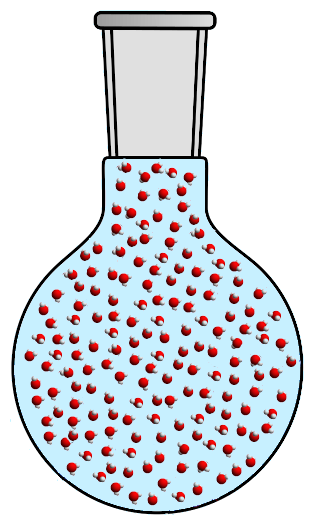
Lorsque l’on avait du gaz et du liquide bien séparés, la gravité maintenait la phase liquide en bas et la phase gazeuse en haut. Si les deux phases sont de densités égales, l’interface disparaît. Il n’y a plus de liquide, il n’y a plus de gaz : tout n’est alors que fluide supercritique.
Pour obtenir un fluide supercritique en chauffant une bouteille fermée, il faut qu’il y ait assez de liquide dans la bouteille. Autrement, tout le liquide se transforme en gaz avant d’avoir atteint le point critique et on aurait simplement du gaz chaud. Il faut qu’à la température critique, il reste du liquide non évaporé. Le passage d’une situation liquide + gaz à une phase supercritique est très rapide, brusque même : en l’espace d’un instant, les deux phases disparaissent au profit d’une seule, transitant par un bref moment où les deux phases se troublent à cause des transferts de molécules d’une phase à l’autre.
Si l'on rabaisse la pression et la température, une partie du fluide va se contracter et redevenir liquide. Le liquide va retomber au fond de la bouteille et on observe de nouveau deux phases distinctes.
Cette phase supercritique pourrait correspondre à un gaz comprimé à l’extrême, ou un liquide super détendu, mais elle a quand-même des propriétés spécifiques qui la différencient de l’une comme de l’autre.
Propriétés d’un fluide supercritique
Les fluides supercritiques sont de densités intermédiaires entre le liquide et le gaz. Comme on le voit de plus sur les diagrammes de phase, ils sont situés à des températures et des pressions élevées. Pour l’eau, par exemple, il faut monter à 218 bars de pression et 374 °C ! Ce n’est donc pas dans la vie courante que l’on aura de l’eau sous sa forme supercritique.
L’eau supercritique est utilisée pour nettoyer ou désintégrer des déchets variés : les molécules d’eau réussissent à dégrader complètement les matières organiques en molécules plus petites et beaucoup moins toxiques.
Les fluides supercritiques ont généralement aussi des coefficients de viscosité plus faible : leur écoulement est moins sujet à des pertes mécaniques. Certains concepts de générateurs électriques — y compris nucléaires — prévoient l’usage d’eau supercritique pour faire tourner les turbines des réacteurs ou servir de caloporteur, offrant alors une amélioration très sensible du rendement énergétique.
Le dioxyde de carbone supercritique a également des applications dans l’industrie. Il est nettement plus facile à obtenir que l’eau, car il suffit seulement de 74 bars et 31 °C. En plus du nettoyage (à sec) comme pour l’eau et ses propriétés stérilisantes, il est utilisé comme solvant en remplacement avantageux des solvants organiques habituels. Le CO2 supercritique reste du simple CO2 gazeux aussitôt que l’on abaisse la pression et il s’évapore sans laisser de traces.
L’exemple typique est celui de l’extraction de la caféine du café, pour produire du café décaféiné (et de la caféine). La méthode traditionnelle employait des solvants organique, dont il pouvait subsister des traces dans le produit fini, ce qui n’était pas l’idéal. Même remarque dans l’extraction d’arômes et essences ou d’autres molécules végétales dans le domaine de la parfumerie ou celui de la pharmacie.
Inversement, on peut également diluer préalablement des pigments dans du CO2 supercritique en vue de teindre du textile par exemple : cette technologie apporte l’avantage de nécessiter beaucoup moins d’eau et de produits dangereux dans un secteur autrement particulièrement polluant et gourmand en eau.
Un dernier exemple de fluide supercritique, et c’est celui que l’on voit généralement dans les salles de classe ou les musées, c’est l’hexafluorure de soufre supercritique. On l’utilise pour les démonstrations « grand public » car il est très simple à obtenir : « seulement » 38 bar et 46 °C.
Notes
Bien que je parle ici d’obtenir du fluide supercritique dans une bouteille, ce n’est pas possible. En vrai, ce n’est clairement pas une bouteille que l’on utilise, mais des dispositifs spéciaux destinés à résister à des pressions de plusieurs centaines de bars. Les petites vitres pour pouvoir voir le fluide sont généralement en quartz ou en saphir très épais pour pouvoir voir sans que ça ne casse.
Pour info, un pneu de voiture, c’est 2 à 3 bars, une bouteille de soda ou une recharge de gaz 5-7 bars et un extincteur de l’ordre de 15 bars.
N’essayez donc pas de chauffer votre bouteille en verre à la maison : les conditions de pression et de température à obtenir sont beaucoup trop élevées. Vous risqueriez de faire exploser la bouteille et de mettre de l’eau brûlante partout.