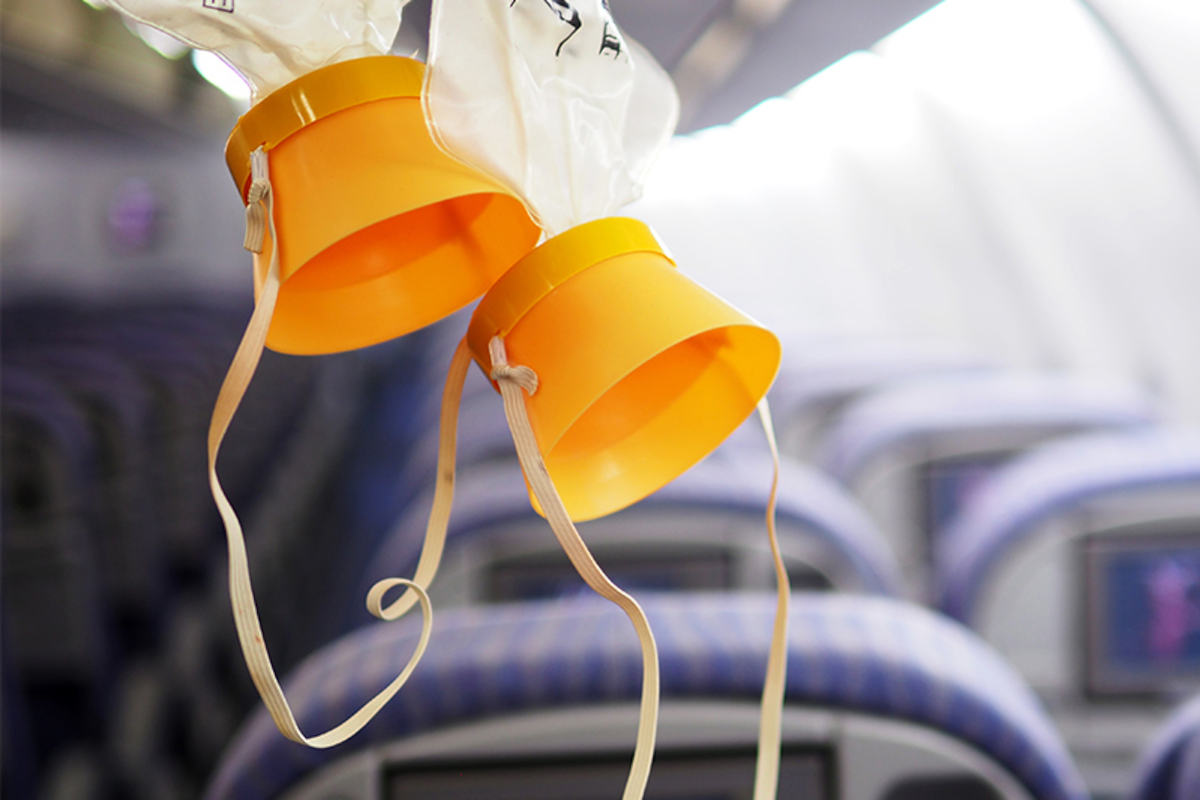
Dans un avion, il vous est toujours demandé d’être attentif aux consignes de sécurité, notamment pour ce qui est des masques à oxygène.
Ces masques sont là pour nous donner de quoi respirer si la cabine venait à se dépressuriser en altitude, où l’air est raréfié. Si ces masques descendent, de l’oxygène permet de respirer durant 20 à 30 minutes, le temps que l’avion descende sous les 10 000 pieds, là où l’air est respirable naturellement.
On pourrait penser que ces masques sont alimentés par de simples bouteilles d’oxygène, mais ce n’est pas le cas : les bouteilles sont lourdes, sous pression, et demandent une surveillance et une maintenance, et sont totalement exagérés pour 20 minutes d’oxygène. Seuls les pilotes peuvent en avoir, dans le cas où ils en auraient besoin plus longtemps que les passagers pour descendre l’avion et le faire atterrir sans risquer de tomber en manque d’oxygène.
Seules quelques lignes (celles qui surpassent l’Himalaya par exemple), embarquent aujourd’hui des bouteilles d’oxygène, car au-dessus des montagnes, il n’est pas possible de descendre sous les 10 000 pieds. Certains avions plus récents (Boeing 787) comportent aussi des bouteilles d’oxygène, mais cela reste une exception.
Une réaction chimique qui produit de l’oxygène à bord !
En cas d’urgence dans un avion en vol, lors d’une dépressurisation de la cabine notamment, les masques tombent du plafond automatiquement. À ce stade, ils ne sont pas encore alimentés. Ce n’est que lorsque l’on tire sur le tuyau que le système s’enclenche. Le tuyau tire en réalité sur une petite goupille, comme celle d’une grenade. Ce n’est qu’une fois dégoupillé que le système de production d’oxygène s’active.
La plupart des avions utilisent des générateurs chimiques à oxygène, aussi appelées bougies à oxygène. Ces générateurs libèrent du dioxygène (O2) grâce à une réaction chimique :
$$ 2\text{NaClO}_3 → 2 \text{NaCl} + 3 \text{O}_2$$
La réaction ici est la décomposition du chlorate de sodium en présence de peroxyde de baryum ou de poudre de fer. Le chlorate de sodium est essentiellement du sel de table enrichie à l’oxygène. Sa décomposition sous l’effet de la température libère cet oxygène comme un produit de la réaction, à raison de 6,5 heures-homme d’oxygène par kilogramme.
C’est cet oxygène que nous respirons quand les masques tombent. Parmi les autres produits de la réaction figurent tout simplement du sel de table, inerte et sans aucun danger.
D’autres métaux du même groupe que le sodium (potassium, lithium) peuvent également être utilisés à la place. De l’oxyde de fer est produit à cause du fer, nécessaire à entretenir la décomposition du chlorate de sodium. La réaction se fait à haute température (600 °C), mais est contenue, généralement dans une bouteille en acier.
Une réaction chimique, par exemple une combustion de bois, d’une bougie ou du gaz domestique (méthane, butane), libère généralement du CO2 et de l’eau (H2O), mais certaines, comme ici, produisent à peu près ce que l’on veut, et dans le cas présent, nous voulons du dioxygène respirable.
En dehors des avions, les pompiers et les services de secours peuvent aussi avoir recours à ces dispositifs, même si, pour les pompiers, les bouteilles qu’ils embarquent sur le dos sont des bouteilles d’air comprimé, pas d’oxygène (ce serait trop dangereux au cœur d’un incendie).
Ces générateurs sont également utilisés dans les sous-marins. Dans la Station Spatiale Internationale (ISS), l’ensemble de ressources fonctionne en cycle fermé : l’eau est récupérée et décomposée en oxygène et en hydrogène (lui-même retraité ensuite avec le CO2 expiré pour fournir du méthane et de l’oxygène). En cas de secours, il y a aussi un système des bougies à oxygène comme dans les avions.
D’autres exemples d’utilisation de générateurs chimiques
Comme dit un peu plus haut, l’on peut prévoir une réaction chimique libérant à peu près le produit que l’on veut. Ici, c’est de l’oxygène utile pour la respiration. Parfois, ce sont d’autres gaz.
Dans les airbags de voitures, par exemple, l’oxygène serait une mauvaise idée : en cas d’accident, le véhicule peut être en feu et l’oxygène ne ferait qu’empirer cela. Il faut que la réaction de libération des gaz soit très rapide (quelques millisecondes), et le gaz doit être inerte. Le système doit de plus être stable dans le temps et ne pas se détériorer durant une vingtaine d’années. La solution retenue est généralement une réaction productrice de diazote. J’explique cela dans mon article sur les airbags.
Ressources et liens
- I Can’t Believe they put THIS onboard! | Valujet flight 592 - YouTube
- TIL that the oxygen for emergency masks on planes does not come from tanks, but instead from a chemical reaction : r/todayilearned
- Planes Don't Carry Tanks Of Oxygen. So What's In Your Emergency Mask?
- Générateur chimique d’oxygène — Wikipédia
- ISS ECLSS